9급 지방직 공무원 화학(2018. 5. 19.) 시험일자 : 2018년 5월 19일
1. 산소와 헬륨으로 이루어진 가스통을 가진 잠수부가 바다 속 60m에서 잠수중이다. 이 깊이에서 가스통에 들어 있는 산소의 부분 압력이 1140mmHg일 때, 헬륨의 부분 압력[atm]은? (단, 이 깊이에서 가스통의 내부 압력은 7.0atm이다)
- ① 5.0
- ② 5.5
- ③ 6.0
- ④ 6.5
등록된 댓글이 없습니다.
2. 다음 각 원소들이 아래와 같은 원자 구성을 가지고 있을 때, 동위 원소는?
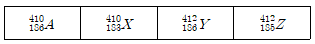
- ① A, Y
- ② A, Z
- ③ X, Y
- ④ X, Z
등록된 댓글이 없습니다.
3. 다음 평형 반응식의 평형 상수 K값의 크기를 순서대로 바르게 나열한 것은?
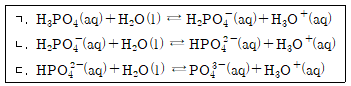
- ① ㄱ>ㄴ>ㄷ
- ② ㄱ=ㄴ=ㄷ
- ③ ㄴ>ㄷ>ㄱ
- ④ ㄷ>ㄴ>ㄱ
등록된 댓글이 없습니다.
4. 방사성 실내 오염 물질은?
- ① 라돈(Rn)
- ② 이산화 질소(NO2)
- ③ 일산화 탄소(CO)
- ④ 폼알데하이드(CH2O)
등록된 댓글이 없습니다.
5. 볼타 전지에서 두 반쪽 반응이 다음과 같을 때, 이에 대한 설명으로 옳지 않은 것은?

- ① Ag는 환원 전극이고 Cu는 산화 전극이다.
- ② 알짜 반응은 자발적으로 일어난다.
- ③ 셀 전압()은 1.261V이다.
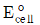
- ④ 두 반응의 알짜 반응식은 이다.
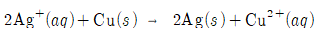
등록된 댓글이 없습니다.
6. 끓는점이 가장 낮은 분자는?
- ① 물(H2O)
- ② 일염화 아이오딘(ICl)
- ③ 삼플루오린화 붕소(BF3)
- ④ 암모니아(NH3)
해설2024. 1. 6. 01:21삭제
https://ywpop.tistory.com/18576
7. 산화수 변화가 가장 큰 원소는?
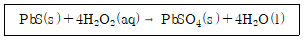
- ① Pb
- ② S
- ③ H
- ④ O
등록된 댓글이 없습니다.
8. 다음 중 분자 간 힘에 대한 설명으로 옳은 것만을 모두 고르면?

- ① ㄱ
- ② ㄴ
- ③ ㄱ, ㄷ
- ④ ㄴ, ㄷ
등록된 댓글이 없습니다.
9. 원자들의 바닥 상태 전자 배치로 옳지 않은 것은?
- ① Co: [Ar]4s13d8
- ② Cr: [Ar]4s13d5
- ③ Cu: [Ar]4s13d10
- ④ Zn: [Ar]4s23d10
등록된 댓글이 없습니다.
10. 체심 입방(bcc) 구조인 타이타늄(Ti)의 단위 세포에 있는 원자의 알짜 개수는?
- ① 1
- ② 2
- ③ 4
- ④ 6
등록된 댓글이 없습니다.
11. 0.50M NaOH 수용액 500mL를 만드는 데 필요한 2.0M NaOH 수용액의 부피[mL]는?
- ① 125
- ② 200
- ③ 250
- ④ 500
등록된 댓글이 없습니다.
12. 다음에서 실험식이 같은 쌍만을 모두 고르면?

- ① ㄱ, ㄷ
- ② ㄱ, ㄹ
- ③ ㄴ, ㄷ
- ④ ㄷ, ㄹ
등록된 댓글이 없습니다.
13. 분자 수가 가장 많은 것은? (단, C, H, O의 원자량은 각각 12.0, 1.00, 16.0이다)
- ① 0.5mol 이산화 탄소 분자 수
- ② 84g 일산화 탄소 분자 수
- ③ 아보가드로 수만큼의 일산화 탄소 분자 수
- ④ 산소 1.0mol과 일산화 탄소 2.0mol이 정량적으로 반응한 후 생성된 이산화 탄소 분자 수
등록된 댓글이 없습니다.
14. 0.30M Na3PO4 10mL와 0.20M Pb(NO3)2 20mL를 반응시켜 Pb3(PO4)2를 만드는 반응이 종결되었을 때, 한계 시약은?
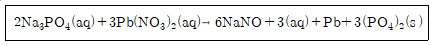
- ① Na3PO4
- ② NaNO3
- ③ Pb(NO3)2
- ④ Pb3(PO4)2
등록된 댓글이 없습니다.
15. 분자식이 C5H12인 화합물에서 가능한 이성질체의 총 개수는?
- ① 1
- ② 2
- ③ 3
- ④ 4
등록된 댓글이 없습니다.
16. 다음 중 산화-환원 반응은?
- ① Na2SO4(aq)+Pb(NO3)2(aq)→PbSO4(s)+2NaNO3(aq)
- ② 3KOH(aq)+Fe(NO3)3(aq)→Fe(OH)3(s)+3KNO3(aq)
- ③ AgNO3(aq)+NaCl(aq)→AgCl(s)+NaNO3(aq)
- ④ 2CuCl(aq)→CuCl2(aq)+Cu(s)
등록된 댓글이 없습니다.
17. 분자 내 원자들 간의 결합 차수가 가장 높은 것을 포함하는 화합물은?
- ① CO2
- ② N2
- ③ H2O
- ④ C2H4
등록된 댓글이 없습니다.
18. 물과 반응하였을 때, 산성이 아닌 것은?
- ① 에테인(C2H6)
- ② 이산화 황(SO2)
- ③ 일산화 질소(NO)
- ④ 이산화 탄소(CO2)
등록된 댓글이 없습니다.
19. 물리량들의 크기에 대한 설명으로 옳은 것은?
- ① 산소(O2) 내 산소 원자 간의 결합 거리>오존(O3) 내 산소 원자 간의 평균 결합 거리
- ② 산소(O2) 내 산소 원자 간의 결합 거리>산소 양이온(O2+) 내 산소 원자 간의 결합 거리
- ③ 산소(O2) 내 산소 원자 간의 결합 거리>산소 음이온(O2-) 내 산소 원자 간의 결합 거리
- ④ 산소(O2)의 첫 번째 이온화 에너지>산소 원자(O)의 첫 번째 이온화 에너지
등록된 댓글이 없습니다.
20. 용액에 대한 설명으로 옳은 것은?
- ① 순수한 물의 어는점보다 소금물의 어는점이 더 높다.
- ② 용액의 증기압은 순수한 용매의 증기압보다 높다.
- ③ 순수한 물의 끓는점보다 설탕물의 끓는점이 더 낮다.
- ④ 역삼투 현상을 이용하여 바닷물을 담수화할 수 있다.
등록된 댓글이 없습니다.